近期,全球多地报告了一种叫做不明原因儿童急性肝炎的疾病,引发广泛关注。
患者大多是10岁以下的儿童,他们会出现黄疸、恶心、腹痛、乏力、嗜睡,以及包括腹泻和呕吐在内的胃肠道症状,大多数患儿无发热;此外,实验室肝生化检查转氨酶(AST或ALT)明显升高[1]。
世界卫生组织(WHO)5月27日发布的报告表明,截至5月26日,33个国家已向该组织报告了650例病因不明的儿童肝炎病例[2]。据此前的报道,已有11名儿童死亡,31名儿童需要肝移植[3]。
遗憾的是,直到现在科学家也不能确定,究竟是什么导致了不明原因的儿童急性肝炎。
新冠病毒感染是幕后黑手?
作为一种急性肝炎,科学家在不明原因的儿童急性肝炎患儿身上没有发现甲型、乙型、丙型、丁型和戊型肝炎病毒。虽然一些患儿体内检测到了腺病毒41F,但是过往的腺病毒感染没有出现过此类病例[4]。
就在科学家一筹莫展的时候,近期的三篇研究论文将矛头指向了新冠病毒感染。
来自英国帝国理工学院的Petter Brodin和他的同事认为,儿童感染新冠病毒后,残存的病毒库可能会导致超级抗原介导的免疫细胞反复激活;如果这些儿童随后又感染了腺病毒,由超级抗原介导的免疫激活作用可能会加强,最终导致急性严重肝炎的发生[4]。
 ▲Petter Brodin提出的假设
▲Petter Brodin提出的假设在Brodin的假说发布一天后,美国凯斯西储大学医学院的研究人员发表了新的证据。他们基于美国患者的电子健康记录(EHR)数据库,分析了近80万1-10岁儿童的数据,结果发现与其他呼吸道感染的儿童相比,感染新冠肺炎的儿童AST或ALT升高风险增加152%[5]。这正是不明原因的儿童急性肝炎的主要实验室表现之一。因此,研究人员认为,有必要进一步研究新冠病毒感染导致的肝损伤与不明原因的儿童急性肝炎之间的关系。
第三个研究来自中科院上海营养与健康研究所,研究人员分析了新冠病毒的序列,发现ORF1ab发生A1061S突变的新冠病毒变异株与人体蛋白PARP14的一段序列高度同源,这会导致新冠病毒通过表位模拟引起患者自身免疫性T细胞反应[6]。
另外,由于儿童外周T细胞耐受处于建立阶段,上述特定变异新冠病毒的感染对系统和局部免疫微环境的干扰,可能影响正常T细胞耐受的建立。这在一定程度上解释了为何不明原因急性肝炎患者都是16岁及以下的儿童。
以上三个研究虽然不能直接证明新冠病毒感染就是不明原因的儿童急性肝炎的原因,但至少提供了一定证据。通过这三篇文章,我们也要认识到,新冠病毒感染还有很多未知的领域,尤其是对儿童。
儿童感染风险不低,但症状轻
WHO发布的最新数据显示,截至今年5月25日,全球累计新冠肺炎感染者超过5.2亿人[7]。
虽然WHO没有发布全球儿童感染的数据,但是从美国儿科学会发布的数据来看,截至今年5月19日,美国累计报告超过1325万名儿童感染病例(占美国儿童总数的18%),占美国确诊病例总数的19%[8]。按照这个比例推算,全球新冠患儿总数应该在1亿左右。
值得注意的是,自奥密克戎变异株大流行以来,美国报告的新冠患儿数量激增,在累计1325万名患儿中,近540万是2022年前几个月确诊的[8]。
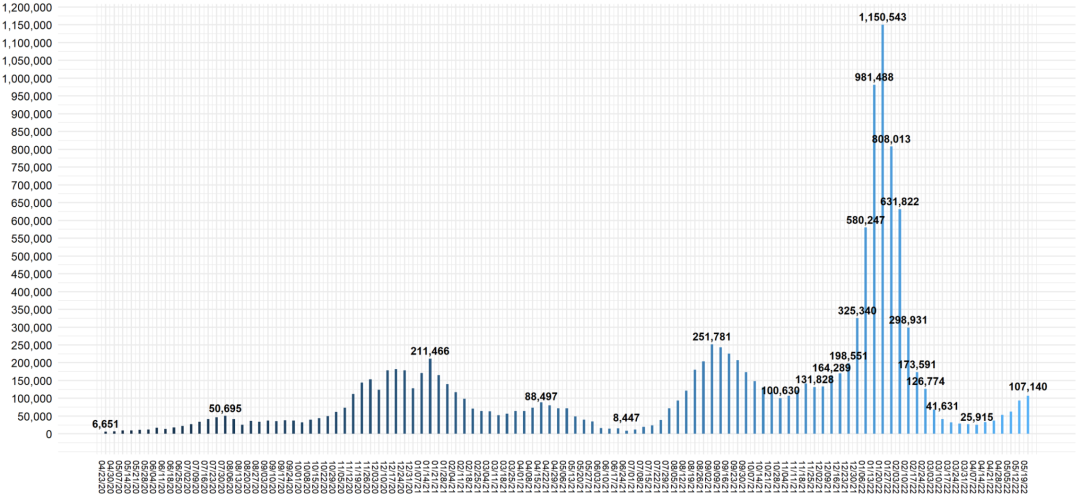 ▲美国每周确诊儿童新冠患者数量[8]
▲美国每周确诊儿童新冠患者数量[8]从上图可以发现,在不同的新冠变异株流行期间,儿童感染新冠也呈现出不同的特点。
2020年9月(德尔塔变异株出现之前),伦敦大学学院Russell M. Viner团队发表了一篇系统性的荟萃分析研究论文[9]。他们分析了32项研究的数据,比较了20岁以下的儿童和青少年,与20岁及以上的成人相比感染新冠肺炎的风险。结果发现,与成人相比,20岁以下的儿童和青少年感染新冠的风险下降了44%,10-14岁人群下降的更明显。这个研究初步证明,与成人相比,儿童和青少年感染新冠的风险稍低。
美国儿科学会发布的数据也在一定程度上证明了上述结论:2020年4月,在所有确诊病例中,儿童仅占2%左右[8]。要知道,美国儿童数量占总人口数量的22.2%。
不过,今年4月份美国疾病控制与预防中心(CDC)发布的一份血清学研究显示,儿童对德尔塔变异株和奥密克戎变异株更易感[10]。在2021年12月至2022年2月期间,美国总体血清流行率从33.5%增加到57.7%。具体来看,0-11岁儿童的血清流行率从44.2%增加到75.2%,12-17岁的青少年从45.6%增加到74.2%,18-49岁的成年人从36.5%增加到63.7%,50-64岁的成年人从28.8%增加到49.8%,65岁及以上的人从19.1%到33.2%。
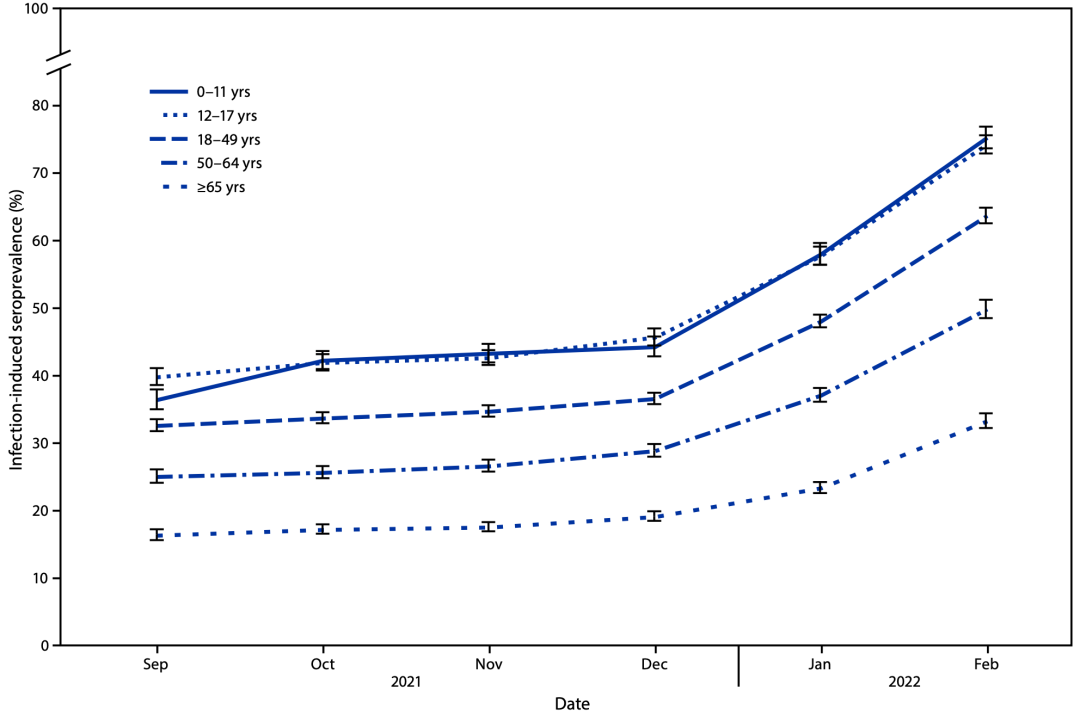 ▲美国新冠感染血清学研究[10]
▲美国新冠感染血清学研究[10]也就是说,截止今年2月,美国可能有四分之三的儿童都感染过新冠病毒,而且这一数据远超其他年龄段人群。结合美国儿科学会发布的1325万名儿童感染病例数据,我们可以推知,儿童虽然更易感德尔塔/奥密克戎变异株,但是大部分儿童感染后症状非常轻,甚至是无症状感染者,这才导致确诊儿童仅占儿童总数的18%。实际上,也有其他研究表明,与成人相比,儿童感染德尔塔/奥密克戎变异株的症状比成年人轻[11]。
同样是在今年4月份,康奈尔大学威尔康奈尔医学院的研究人员发表了一项研究成果[12]。他们发现,在德尔塔变异株的儿童感染者中,84.2%为轻度,15.7%为中度,0.1%为重度/危重症;奥密克戎感染者中,97.8%为轻度,2.2%为中度,无重症/危重症(P
前不久,国家儿童医学中心复旦大学附属儿科医院的研究人员,研究了今年3月7日-31日奥密克戎变异株在上海流行期间,儿童感染奥密克戎的情况。这个研究分析了376例新冠肺炎儿童病例(中位年龄:6.0±4.2岁),其中68.4%的患儿有症状,31.6%的患儿无症状,没有患儿发生重症。对于有症状的患儿,症状主要为发热(83.4%),咳嗽(40.2%),一过性白细胞减少(16.4%)等[13]。
虽然总体上看,儿童感染者症状比较轻,但是从美国儿科学会发布的报告也能看到一个让担心的趋势:在2020年5月到2022年5月之间,尽管儿童新冠感染者的住院率从3.8%降低到0.7%,但住院的新冠感染者的儿童占比却从0.8%增加到3.2%[8]。
以上数据说明,美国儿童感染率在快速上升,虽然住院率低,但是感染基数大,导致住院人数增多,所以在总住院人数中儿童的占比增加了3倍。在所有的儿童新冠症状中,最需要注意的是新冠肺炎相关的儿童多系统炎症综合征(MIS-C)。
警惕儿童多系统炎症综合征(MIS-C)
在2020年春季,欧洲的一些国家开始出现疑似川崎病的儿童病例,由于与往年相比发病率大大增加,且症状不典型,这引起了研究人员的注意。
后来的免疫学分析发现,这些患者的病理特征不同于川崎病,也不同于重症新冠肺炎的细胞因子风暴,而是另一种多系统炎症综合征。现在这个症状被定义为儿童多系统炎症综合征(MIS-C)。
美国CDC对儿童多系统炎症综合征的定义为,同时满足下列三个条件[14]:①年龄在21岁以下,表现为发烧(超过38.0°C长达24小时或更长时间,或报告主观发烧持续24小时或更长时间),实验室炎症证据(包括但不限于以下一项或多项症状:C反应蛋白、红细胞沉降率、纤维蛋白原、降钙素原、d-二聚体、铁蛋白、乳酸脱氢酶或白细胞介素6升高,中性粒细胞升高,淋巴细胞减少,白蛋白降低),以及需要住院治疗的临床严重疾病证据,具有多系统(≥2)器官损害(心脏、肾脏、呼吸、血液、胃肠、皮肤或神经);②没有其他合理的诊断;③通过RT-PCR、血清学或抗原检测,当前或最近的新冠病毒感染呈阳性;或在症状出现前的4周内接触过疑似或确诊新冠肺炎病例。
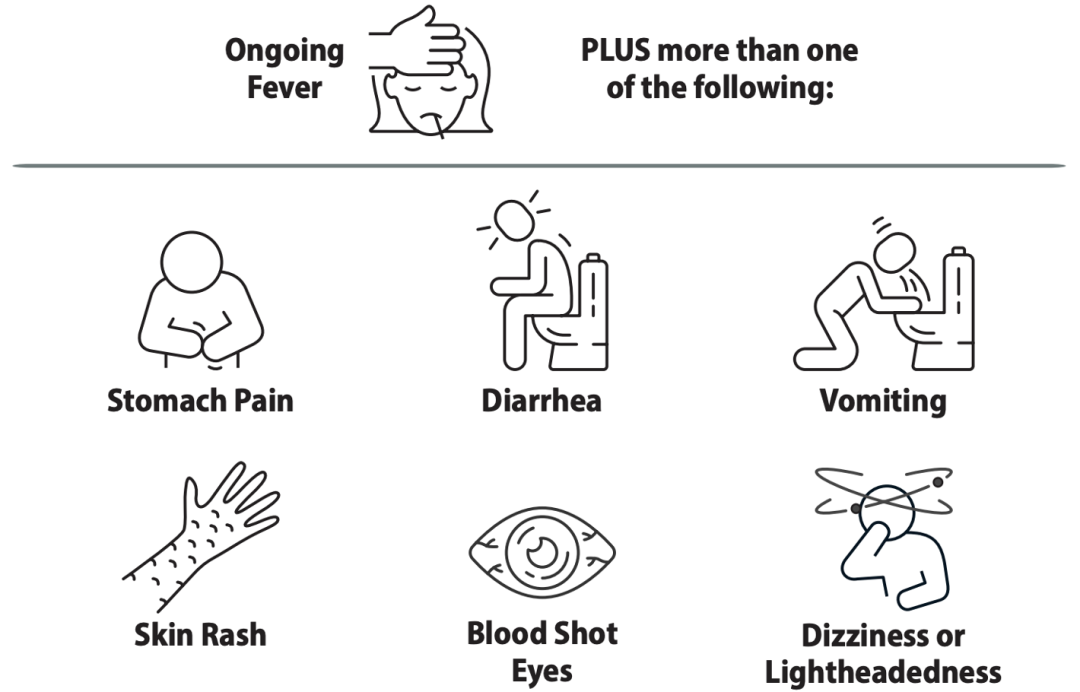 ▲如何识别儿童多系统炎症综合征[15]
▲如何识别儿童多系统炎症综合征[15]儿童多系统炎症综合征患儿通常表现为持续发热、腹痛、呕吐、腹泻、皮疹、皮肤黏膜病变,严重时会出现低血压和休克,甚至死亡[14]。他们的炎症实验室标志物(例如C反应蛋白、铁蛋白)会升高,大多数患者的心脏损伤实验室标志物(例如肌钙蛋白、B型利钠肽等)会升高。一些患者会出现心肌炎、心功能不全和急性肾损伤[14]。
需要指出的是,儿童多系统炎症综合征可能在儿童感染新冠病毒数周(3-6周)后开始,无症状感染者也有可能发展成为儿童多系统炎症综合征[14]。
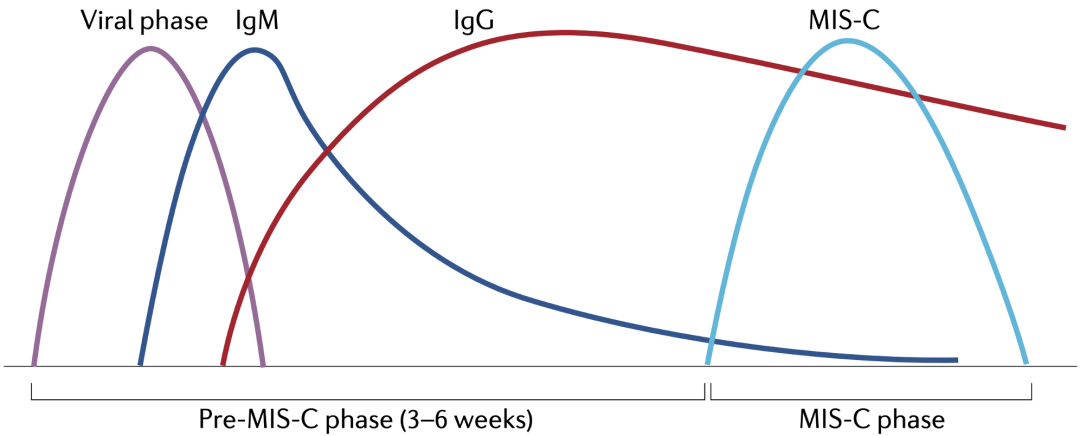 ▲儿童多系统炎症综合征发生的时期[16]
▲儿童多系统炎症综合征发生的时期[16]本月初,美国CDC发布了截至今年5月2日累计儿童多系统炎症综合征患者的数据,累计8210名患儿确诊为儿童多系统炎症综合征,其中68名患儿因此死亡[17]。所有儿童多系统炎症综合征患者的中位年龄为9岁,半数患有儿童多系统炎症综合征的儿童年龄在5至13岁之间。其中98%的患儿新冠病毒检测结果呈阳性,其余的患者与新冠肺炎患者有过接触[17]。
同一时期,美国累计确诊儿童新冠病例1300万左右,累计住院超过4万例,累计死亡超过1000例[8]。不难看出,多系统炎症综合征的发病率虽然低,但是占重症和死亡的比例并不低。
至于为何这种多系统炎症综合征只出现在儿童和年轻人身上,而不出现在中老年人身上,还没有确切的解释。不过,目前已经有一些可能的推测[11],例如,新冠病毒感染带来的超抗原介导了T细胞的活化,而且新冠病毒在儿童和成人体内引发的初始免疫反应可能有所不同,还有研究暗示,与新冠病毒在儿童和成年人肠道的存留时间差异有关,以及与HLA I的遗传背景和T细胞免疫耐受的建立等有关。
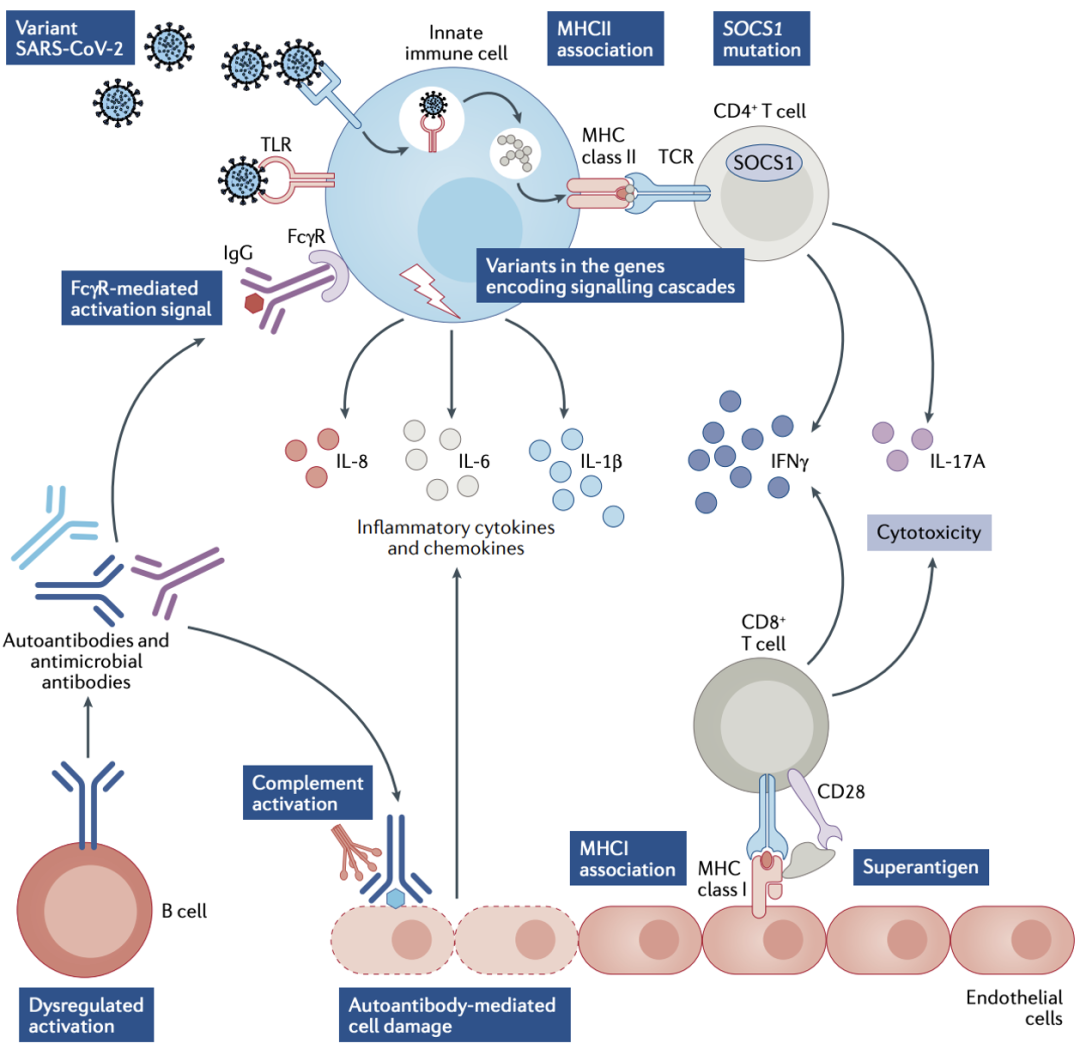 ▲儿童多系统炎症综合征免疫层面的可能机制[16]
▲儿童多系统炎症综合征免疫层面的可能机制[16]前不久,来自以色列Rambam医学中心的研究人员,研究了阿尔法、德尔塔和奥密克戎变异株流行期间儿童多系统炎症综合征发生情况[18]:在阿尔法变异株流行期间,18岁以下儿童的多系统炎症综合征发病率为54.5/10万,在德尔塔变异株流行期间这一数据为49.2/10万,而奥密克戎变异株流行期间这一数据仅为3.8/10万。
虽然感染奥密克戎变异株后儿童多系统炎症综合征的发病率较低,但是奥密克戎变异株的感染能力更强,感染的儿童会更多,因此仍会有很有儿童可能会发生多系统炎症综合征。
那如何预防儿童多系统炎症综合征呢?从源头上说,儿童多系统炎症综合征是新冠病毒感染引起的,因此能预防新冠感染的办法就能预防儿童多系统炎症综合征。
接种疫苗是最好的保护
美国CDC发布的一份报告显示,新冠疫苗免疫接种可将12-18岁青少年患多系统炎症综合征的风险降低91%。在12-18岁因儿童多系统炎症综合征而住院治疗的患者中,有95%没有接种疫苗[19]。
 ▲新冠疫苗的保护效果[19]
▲新冠疫苗的保护效果[19]遗憾的是,目前还没有新冠疫苗预防12岁以下儿童患多系统炎症综合征有效性的数据,随着12岁以下儿童接种疫苗的人数越来越多,相关的数据肯定也会出炉。不过,近期丹麦的一项真实世界队列研究显示,接种疫苗对5-17岁的儿童预防多系统炎症综合征的效果为94%[20]。
事实上,目前已经有大量临床试验表明,儿童接种新冠疫苗的安全性良好,且对预防感染新冠有一定的效果,并可显著降低重症发生风险。
例如,今年5月中旬发表的一项研究表明,接种BNT162b2疫苗后,5至11岁儿童因奥密克戎变异株有关的住院风险降低了68%;在12至18岁的青少年中,两剂疫苗预防奥密克戎相关的住院有效性为40%,但预防重症的有效性为79%[21]。
同样是在今年5月份,美国CDC发表的另一项研究发现[22],在奥密克戎变异株流行期间,5-11岁的儿童接种两剂BNT162b2后的2-4周,预防有症状感染的有效性为60.1%,接种后2个月时有效性下降到28.9%;对于12-15岁的青少年而言,上述两个数据分别为59.5%和16.6%。不过,12-15岁的青少年接种加强针后的2-6.5周,疫苗的有效性上升到71.1%。
除了mRNA疫苗之外,灭活疫苗在保护儿童感染新冠上有一定的效果。同样是今年的5月中旬,来自智利的一项研究,评估了灭活疫苗CoronaVac对3至5岁儿童的保护效果[23]。研究结果表明,在奥密克戎变异株流行期间,两剂CoronaVac对有症状的新冠肺炎的保护效果为38.2%,对住院的保护效果为64.6%,对入住ICU的保护效果为69.0%。
值得一提的是,今年3月份,来自以色列医疗服务机构克拉利特研究所的研究人员在《科学》杂志上发表的一项研究成果表明[24],父母一方接种疫苗与12岁及以下未接种疫苗儿童感染风险下降26%有关,而父母双方接种疫苗与未接种疫苗儿童感染风险下降71.7%有关。
 ▲父母接种疫苗可以保护儿童[24]
▲父母接种疫苗可以保护儿童[24]不难看出,父母接种疫苗对家庭中未接种疫苗的儿童有很大的保护作用。所以还未接种疫苗的父母们,不要再犹豫了,赶快接种疫苗。
除了接种疫苗之外,在之前的文章中,我们还介绍过洗手、戴口罩和物理隔离这三种公共卫生预防措施预防新冠感染的效果。澳大利亚莫纳什大学科学家在《英国医学杂志》(BMJ)发表的一篇系统评价和荟萃分析的研究论文[25]表明,洗手、戴口罩和物理隔离都能不同程度地降低新冠肺炎感染风险。
 ▲公共卫生预防措施预防新冠的效果[25]
▲公共卫生预防措施预防新冠的效果[25]不过需要注意的是,公共卫生措施虽然也能预防新冠感染,但是对于儿童而言,物理隔离还会带来一些不易察觉的影响,例如学校停课会对学生的社会、心理和教育产生不利的影响等[26]。
不害怕,不着急,有药可医
公共卫生措施和新冠疫苗,虽然给儿童提供了保护,但是仍不能完全避免感染新冠。如果儿童感染了新冠肺炎,又该如何治疗呢?
在全球范围内,曾被推荐用于轻型和普通型,且伴有进展为重型高风险因素患者的药物主要有两类。一类是小分子药物,例如Paxlovid(奈玛特韦片/利托那韦片组合包装),Remdesivir和Molnupiravir;另一类是单抗隆中和抗体Bebtelovimab,Bamlanivimab/Etesevimab,Sotrovimab和安巴韦单抗/罗米司韦单抗等。
小分子药物方面,Remdesivir注射液在儿童中的适用范围最大,可以用于出生28天或体重在3公斤以上的儿童新冠肺炎患者,儿童患者的用药剂量需要根据年龄和体重调整[27]。不过Remdesivir目前没有在中国获批。Paxlovid被FDA批准可用于12-17岁且体重40公斤以上的儿科患者,但是不推荐合并重度肝肾功能不全(eGFR的患者使用;也不推荐与高度依赖CYP3A进行清除,且其血浆浓度升高会导致严重和/或危及生命的不良反应的药物联用[27]。另外,Paxlovid虽然已经在中国获批了,但是没有用于12-17岁且体重40公斤以上的青少年这个适应证[28]。
曾经获得过FDA批准的抗新冠病毒中和抗体有很多,它们均可用于12-17岁且体重40公斤以上的青少年,不过由于奥密克戎变异株的流行,大部分中和抗体被停用。值得一提的是,Bamlanivimab/Etesevimab这对中和抗体组合之前不仅获批用于青少年人群,还可以用于轻中度新冠肺炎儿童患者(包括体重1公斤及以上新生儿)的治疗,对于18岁以下但体重在40公斤以上的儿童,用药剂量与成人一样;体重为40公斤及以下的儿童才需要按照体重调整给药剂量[29]。
与小分子药物不同,中和抗体的使用不受肝肾功能的影响,而且临床研究数据也表明,Bamlanivimab/Etesevimab在儿童患者中的治疗相关不良反应的发生率与安慰剂组相当,没有发生率超过1%的治疗相关不良反应出现[29]。
今年3月份,来自意大利罗马Bambino Gesù儿童医院的研究人员研究了出生24天到18岁的新冠患儿使用单克隆中和抗体治疗的安全性[30]。这个研究一共纳入了73名0-18岁的轻中度且有重症危险因素的新冠患儿,其中最常见的合并症是继发性免疫缺陷和先天性心脏病。总的来看,所有接受治疗的患者没有出现明显的副作用或需要停止输注的不良反应。
从以上的内容可以看出,抗新冠病毒中和抗体在儿童中应用是相对安全的。
 ▲电镜下的新冠病毒(图源:NIAID-RML)
▲电镜下的新冠病毒(图源:NIAID-RML)目前我国唯一获批的中和抗体组合是安巴韦单抗/罗米司韦单抗,它们被批准用于治疗轻型和普通型且伴有进展为重型(包括住院或死亡)高风险因素的成人和青少年(12—17岁,体重≥40kg)新型冠状病毒感染(COVID-19)患者。其中,青少年(12—17岁,体重≥40kg)适应症人群为附条件批准[31]。目前看来,安巴韦单抗/罗米司韦单抗这对抗病毒中和抗体组合也是国内唯一能用于治疗青少年新冠肺炎患者的药物。
总的来说,儿童感染新冠病毒的风险并不低,尤其是在奥密克戎变异株流行的时期;不过,儿童感染者症状相对成人要轻,无症状感染者非常多。尽管如此,还是不能掉以轻心,因为有一定比例的患儿会进展为凶险的儿童多系统炎症综合征。此外,儿童感染新冠病毒后,也有后遗症风险,不过目前相关数据较少,还需要更深入的研究。
对于儿童而言,无论是预防新冠感染,还是预防儿童多系统炎症综合征,接种新冠疫苗都是最好的保护措施。如果因为特殊的原因,例如年龄不够等,不能接种疫苗,儿童的父母接种也可以降低儿童感染新冠的风险。
因此,我们这里再次呼吁大家,如果条件允许,一定要接种疫苗。毕竟这才是在新冠疫情年代对孩子最好的保护。
参考文献:
[1].http://www.nhc.gov.cn/cms-search/xxgk/getManuscriptXxgk.htm?id=d1a3f433743144ddaca5e40b232820b1
[2].https://mp.weixin.qq.com/s/19X1sihlkW9zbDB1vIFRDw
[3].Cevik M, Rasmussen AL, Bogoch II, Kindrachuk J. Acute hepatitis of unknown origin in children. BMJ. 2022;377:o1197. doi:10.1136/bmj.o1197
[4].Brodin P, Arditi M. Severe acute hepatitis in children: investigate SARS-CoV-2 superantigens. Lancet Gastroenterol Hepatol. 2022;S2468-1253(22)00166-2. doi:10.1016/S2468-1253(22)00166-2
[5].Kendall E K, Olaker V R, Kaelber D C, et al. Elevated liver enzymes and bilirubin following SARS-CoV-2 infection in children under 10[J]. medRxiv, 2022.
[6].Wang Y, Liu Y. SARS-CoV-2 ORF1abA1061S potentiate autoreactive T cell responses via epitope mimicry: an explanation to hepatitis of unknown cause[J]. bioRxiv, 2022.
[7].https://www.who.int/emergencies/diseases/novel-coronavirus-2019
[8].https://www.aap.org/en/pages/2019-novel-coronavirus-covid-19-infections/children-and-covid-19-state-level-data-report/
[9].Viner RM, Mytton OT, Bonell C, et al. Susceptibility to SARS-CoV-2 Infection Among Children and Adolescents Compared With Adults: A Systematic Review and Meta-analysis. JAMA Pediatr. 2021;175(2):143-156. doi:10.1001/jamapediatrics.2020.4573
[10].Clarke KE, Jones JM, Deng Y, et al. Seroprevalence of Infection-Induced SARS-CoV-2 Antibodies — United States, September 2021–February 2022. MMWR Morb Mortal Wkly Rep 2022;71:606-608. DOI: http://dx.doi.org/10.15585/mmwr.mm7117e3.
[11].Brodin P. SARS-CoV-2 infections in children: Understanding diverse outcomes. Immunity. 2022;55(2):201-209. doi:10.1016/j.immuni.2022.01.014
[12].Butt AA, Dargham SR, Loka S, et al. COVID-19 Disease Severity in Children Infected with the Omicron Variant. Clin Infect Dis. 2022;ciac275. doi:10.1093/cid/ciac275
[13].Wang X, Chang H, Tian H, et al. Epidemiological and clinical features of SARS-CoV-2 Infection in children during the outbreak of Omicron Variant in Shanghai, March 7-March 31, 2022[J]. medRxiv, 2022.
[14].https://www.cdc.gov /mis/mis-c/hcp/index.html
[15].https://www.cdc.gov/mis/mis-c/hcp/provider-resources/symptoms.pdf
[16].Sharma C, Ganigara M, Galeotti C, et al. Multisystem inflammatory syndrome in children and Kawasaki disease: a critical comparison. Nat Rev Rheumatol. 2021;17(12):731-748. doi:10.1038/s41584-021-00709-9
[17].https://covid.cdc.gov/covid-data-tracker/mis-national-surveillance
[18].Levy N, Koppel JH, Kaplan O, et al. Severity and Incidence of Multisystem Inflammatory Syndrome in Children During 3 SARS-CoV-2 Pandemic Waves in Israel. JAMA. 2022;10.1001/jama.2022.8025. doi:10.1001/jama.2022.8025
[19].https://www.cdc.gov/mmwr/volumes/71/wr/mm7102e1.htm
[20].Nygaard U, Holm M, Hartling UB, et al. Incidence and clinical phenotype of multisystem inflammatory syndrome in children after infection with the SARS-CoV-2 delta variant by vaccination status: a Danish nationwide prospective cohort study. Lancet Child Adolesc Health. 2022. doi:10.1016/S2352-4642(22)00100-6
[21].Price AM, Olson SM, Newhams MM, et al. BNT162b2 Protection against the Omicron Variant in Children and Adolescents. N Engl J Med. 2022;386(20):1899-1909. doi:10.1056/NEJMoa2202826
[22].Fleming-Dutra KE, Britton A, Shang N, et al. Association of Prior BNT162b2 COVID-19 Vaccination With Symptomatic SARS-CoV-2 Infection in Children and Adolescents During Omicron Predominance. JAMA. 2022. doi:10.1001/jama.2022.7493
[23].Jara A, Undurraga EA, Zubizarreta JR, et al. Effectiveness of CoronaVac in children 3 to 5 years during the SARS-CoV-2 Omicron outbreak in Chile. Nat Med. 2022;10.1038/s41591-022-01874-4. doi:10.1038/s41591-022-01874-4
[24].Hayek S, Shaham G, Ben-Shlomo Y, et al. Indirect protection of children from SARS-CoV-2 infection through parental vaccination. Science. 2022;375(6585):1155-1159. doi:10.1126/science.abm3087
[25].Talic S, Shah S, Wild H, et al. Effectiveness of public health measures in reducing the incidence of covid-19, SARS-CoV-2 transmission, and covid-19 mortality: systematic review and meta-analysis. BMJ. 2021;375:e068302. Published 2021 Nov 17. doi:10.1136/bmj-2021-068302
[26].https://www.nature.com/articles/d41586-022-01387-7
[27].https://www.aap.org/en/pages/2019-novel-coronavirus-covid-19-infections/clinical-guidance/outpatient-covid-19-management-strategies-in-children-and-adolescents/
[28].http://www.nhc.gov.cn/yzygj/s7653p/202203/acbffef3d9b74d8ba90e43f8ab091512.shtml
[29].https://www.fda.gov/media/145802/download
[30].Romani L, Calò Carducci FI, Chiurchiù S, et al. Safety of Monoclonal Antibodies in Children Affected by SARS-CoV-2 Infection. Children (Basel). 2022;9(3):369. Published 2022 Mar 7. doi:10.3390/children9030369
[31].https://www.nmpa.gov.cn/yaowen/ypjgyw/20211208212528103.html
感谢您的来访,获取更多精彩文章请收藏本站。










暂无评论内容